دواء زولجنسما (Zolgensma) بمادته الفعالة (onasemnogene abeparvovec-xioi) علاج بديل للجينات، يُستخدَم لعلاج ضمور العضلات الشوكي الذي يصيب الأطفال، بتكلفة 2.1 مليون دولار للجرعة الواحدة العلاجية. دواء زولجنسما حالياً أغلى دواء في الولايات المتحدة. فلماذا تُكلف بعض الأدوية هذا الكمّ الهائل من الأموال، ولماذا يُكلف هذا الدواء 2.1 مليون دولار للجرعة الواحدة؟ وكيف تخطط شركة واحدة لتغيير ذلك؟ هذا ما سنعرفه في هذا المقال، لكن دعونا أولاً نتعرف سريعاً إلى مرض ضمور العضلات الشوكي.
ما مرض ضمور العضلات الشوكي؟
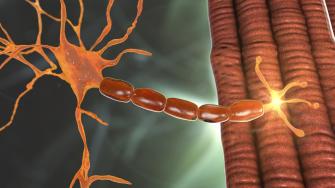
يشير ضمور العضلات الشوكي إلى مجموعة من الأمراض الوراثية التي تدمر وتقتل الخلايا العصبية المتخصصة في الدماغ والحبل الشوكي وتُسمى (الخلايا العصبية الحركية Motor neurons)، وتتحكم الخلايا العصبية الحركية بحركة الذراعين والساقين والوجه والصدر والحلق واللسان، بالإضافة إلى نشاط العضلات الهيكلية، بما في ذلك التحدث والمشي والبلع والتنفس.
بالتالي، عند إصابة الأطفال بإحدى حالات المرض، قد يؤدي ذلك إلى ارتخاء العضلات وضعفها وضمورها، فيصبح الطفل غير قادر على التحكم في حركات رأسه، وأيضاً سيجد صعوبة في الزحف والمشي والبلع، وقد تتطور الحالة وتُصاب العضلات المستخدمة في جهاز التنفس، فيعاني الطفل من صعوبة في التنفس، ما يؤدي إلى وفاة الطفل عند تدهور الحالة.
يظهر المرض عموماً في وقت مبكر من الحياة، وهو السبب الجيني الرئيسي للوفاة عند الرضع والأطفال الصغار، ويُصيب ما يصل إلى 10,000 إلى 25,000 من الأطفال والبالغين في الولايات المتحدة، وبالتالي هو أحد أكثر الأمراض النادرة شيوعاً، حيث يُولد واحد من كل 6000 إلى واحد من كل 10,000 طفل مصاباً بهذا المرض.
هل هناك عدة أنواع لمرض ضمور العضلات الشوكي؟
الشكل الأكثر شيوعاً من ضمور العضلات الشوكي يكون بسبب جين غير طبيعي أو مفقود يعرف باسم جين الخلايا العصبية الحركية 1survival motor neuron gene 1 (SMN1) ، وهذا الجين هو المسؤول عن إنتاج بروتين أساسي للخلايا العصبية الحركية، وهو ضروري لصحة الخلايا العصبية في الحبل الشوكي وبقائها على قيد الحياة.
يختلف تشخيص المرض حسب شكل ونوع ضمور العضلات الشوكي، حيث تكون بعض الأنواع قاتلة دون علاج، وهناك بعض الحالات تكون مستقرة لفترات طويلة، لكن للأسف لا نتوقع أي تحسن دون علاج، وينقسم مرض ضمور العضلات الشوكي إلى أربعة أنواع:
- النوع الأول: الذي يُطلق عليه أيضاً مرض Werdnig-Hoffman))، وعادة ما يصيب الأطفال حديثي الولادة في أول ستة أشهر من العمر، ومن دون علاج يموت العديد من الأطفال المصابين قبل سنّ السنتين.
- النوع الثاني: عادة ما يُلاحَظ هذا النوع من ضمور العضلات الشوكي لأول مرة بين الشهر السادس والشهر الـ 18 من العمر، وينخفض متوسط العمر المتوقع، لكن معظم الأفراد يعيشون لسن المراهقة أو الشباب.
- النوع الثالث: ويطلق عليه (Kugelberg-Welander disease) ويظهر في الأطفال بعد سنّ 18 شهراً، ومع العلاج يمكن أن يتمتع معظم الأفراد بعمر طبيعي.
- النوع الرابع: يحدث في البالغين، وتظهر الأعراض بعد سنّ 21 عاماً، وعادة ما تتطور الأعراض ببطء شديد، وغالباً لا يؤدي إلى الوفاة.
هناك بعض الدراسات التي تشير إلى نوع آخر من أشكال ضمور العضلات الشوكي، لكنه النوع الأخطر والأكثر نُدرة، ويطلق عليه النوع رقم 0، ويتطور هذا النوع في أثناء الحمل، حيث يتحرك الأطفال المصابون بهذا النوع بشكل أقل في الرحم، ويولدون بمشاكل في المفاصل وضعف في العضلات وعضلات التنفس، وغالباً لا يبقون على قيد الحياة بسبب مشاكل في التنفس.
هل يوجد علاج لمرض ضمور العضلات الشوكي؟
بالنسبة إلى علاج مرض ضمور العضلات الشوكي، لا يوجد علاج نهائي للمرض، بل يتكون العلاج من التحكم في الأعراض والوقاية من المضاعفات، إلى أن وافقت منظمة إدارة الغذاء والدواء (FDA) على استخدام دواء نوسينرسين nusinersen تحت الاسم التجاري سبينرازا (Spinraza), ليكون هذا الدواء أول علاج معتمد لضمور العضلات الشوكي على الإطلاق في عام 2016، ويُعطى من طريق الحقن في السائل الذي يحيط بالحبل الشوكي.
ثم وافقت منظمة إدارة الغذاء والدواء في مايو 2019 على العلاج الجيني لدواء زولجنسما (Zolgensma) للأطفال الذين تقلّ أعمارهم عن عامين، ويُحسن فرصتهم للبقاء على قيد الحياة، فهو يعتبر العلاج الوحيد للمرض الذي من الممكن أن يقتلع هذا المرض من جذوره. ثم ظهر أيضاً في عام 2020 دواء ريسديبلامrisdiplam تحت الاسم التجاري (Evrysdi)، وهو الدواء الأول والوحيد المعتمد من قبل إدارة الغذاء والدواء الذي يمكن تناوله في المنزل ومن طريق الفم.
وقبل أن نختص في حديثنا بهذا المقال عن دواء زولجنسما، يجب علينا معرفة أن مرض ضمور العضلات الشوكي عبارة عن مرض طرفي يؤثّر بحركة العضلات، ويؤدي إلى حدوث ضمور لها، لكنه لا يؤثّر في المخ، وبالتالي لا يتأثر النمو الذهني للأطفال المصابين بالمرض، ويكون الطفل طبيعياً مثل باقي الأطفال الطبيعيين في هذا العمر، ومن هنا يجب علينا دعم الأطفال المصابين بمرض ضمور العضلات الشوكي وتشجيعهم وإشراكهم في الأنشطة الحياتية والاجتماعية كافة مثل باقي الأطفال.
ما هو دواء زولجنسما؟ وما هي آلية عمله؟
دواء زولجنسما علاج جيني يستخدم لعلاج ضمور العضلات الشوكي، الذي يحدث عادة عندما يكون جين يسمي SMN1 مفقوداً أو لا يعمل بشكل صحيح، ويقوم دواء زولجنسما بمادته الفعالة (onasemnogene abeparvovec-xioi) بعلاج السبب الجيني الجذري لضمور العضلات من طريق استبدال جين SMN1 المفقود أو الذي لا يقوم بوظيفته بنسخة جديدة عاملة من جين SMN بشري.
يقوم الدواء بذلك باستخدام ناقل في ما يُعرَف بـ vector، ويعتبر هو الناقل الذي يمكنه إدخال جين SMN1 الجديد العامل في الجسم، ويكون الناقل في هذه الحالة فيروساً يُسمى (adeno-associated virus 9 (AAV9، وقد أُزيل الحمض النووي الخاص به واستُبدِل بجين SMN1، وبالتأكيد هذا النوع من الفيروسات لا يجعل الشخص مريضاً، لكن يمكن أن ينتقل بسرعة عبر الجسم إلى الخلايا العصبية الحركية وتوصيل الجين الجديد.
يقع دواء زولجنسما داخل نواة الخلية العصبية الحركية ويُخبرها بالبدء بصنع بروتين SMN1 جديد، وبمجرد وصول الجينات إلى وجهتها، تُفكَّك النواقل وتُخرَج من الجسم ولا تصبح جزءاً من الحمض النووي للطفل، ومن هنا بعد تصنيع البروتين سيبدأ وصول التغذية السليمة للأعصاب الحركية، وبالتالي ستبدأ عضلات الطفل بالحركة بشكل سليم.
كيفية استخدام دواء زولجنسما؟
دواء زولجنسما علاج جيني يُصرف بوصفة طبية للاستخدام في علاج الأطفال الذين تقلّ أعمارهم عن عامين، المصابين بضمور العضلات الشوكي، ويُحقَن الدواء في الوريد مرة واحدة فقط بطريقة التسريب الوريدي ((IV infusion لمدة 60 دقيقة.
يؤخَذ الدواء جنباً إلى جنب مع الكورتيكوستيرويد، العلاج بالكورتيكوستيرويد يكون بجرعة تعادل جرعة دواء بريدنيزولون ((predinisolone من طريق الفم تبلغ 1 مجم/ كجم من وزن الجسم، ويبدأ أخذه قبل أخذ دواء زولجنسما بيوم واحد، ويستمر يومياً لـمدة 30 يوماً على الأقل، حيث يساعد تناول الكورتيزون مع دواء زولجنسما على منع ارتفاع إنزيمات الكبد التي من الممكن أن تؤدي إلى تلف خطير في الكبد.
ما الآثار الجانبية لدواء زولجنسما؟
أكثر الآثار الجانبية شيوعاً التي حدثت في المرضى الذين عولجوا بدواء زولجنسما هي:
- ارتفاع انزيمات الكبد
- القيء
بالتأكيد، هناك آثار جانبية أخرى محتملة. فبالرغم من التأثير الفعال والضروري لـدواء زولجنسما، إلا أنه قد يسبب بعض الآثار الجانبية غير المرغوب فيها. وعلى الرغم من عدم حدوث كل هذه الآثار الجانبية، إلا أنها قد تحتاج إلى عناية طبية في حالة حدوثها، وبالتالي يجب استشارة الطبيب على الفور في حالة حدوث أي من الآثار الجانبية الآتية في أثناء تناول الدواء.
- تغير في لون البراز
- تغير لون البول إلى اللون الداكن
- فقدان الشهية والشعور بتعب غير عادي وإرهاق
- الإصابة بحمى وصداع
- الإصابة بحكة وطفح جلدي
- ألم في المعدة
- تورم في القدمين أو أسفل الساقين
- اصفرار العين أو الجلد
ما الاحتياطات اللازمة عند استخدام دواء زولجنسما؟
قبل البدء باستخدام دواء زولجنسما، يجب على الطبيب التحدث مع عائلة الطفل عن:
- التطعيمات، لتقرير ما إذا كانت هناك حاجة إلى تعديلات على جدول التطعيم، وذلك لاستيعاب العلاج بالكورتيكوستيرويد.
- الوقاية من فيروس الجهاز التنفسي المخلوي respiratory syncytial virus (RSV)، حيث يجب على الطبيب الحفاظ على الطفل من الإصابة بحدوث عدوى فيروسية بالجهاز التنفسي قبل أخذ الحقنة وبعده، لتجنب حدوث مضاعفات ومشاكل خطيرة للطفل عند تناول الدواء، ويجب أيضاً على عائلة الطفل الاتصال بالطبيب المختص على الفور إذا لوحظت أي علامات على عدوى محتملة مثل السعال أو الأزيز أو العطاس أو سيلان الأنف أو التهاب الحلق أو الحمى.
- من الممكن أن يحدث انخفاض في عدد الصفائح الدموية بعد الحقن الوريدي لدواء زولجنسيما، وبالتالي يجب على عائلة الطفل طلب عناية طبية فورية إذا تعرض المريض لنزف أو كدمات غير متوقعة.
- من الممكن أن يحدث اعتلال الأوعية الدقيقة الخثاري أو ما يعرف بـ (Thrombotic microangiopathy (TMA الذي ممكن حدوثه إذا تعرض المريض لنزف أو كدمات غير متوقعة. وتحدث هذه المضاعفة بعد أسبوع واحد تقريباً من أخذ حقنة زولجنسما، بالتالي اذا ظهرت على المريض أي علامات أو أعراض لتلك الحالة مثل الكدمات أو النزف غير المتوقع أو نوبات أو انخفاض كمية البول، يجب تقديم العناية الطبية الفورية له، ومن الأفضل القيام بعمل تحليل بول وصورة دم كاملة (CBC) بعد أسبوع من أخذ الدواء.
- ارتفاع مستويات إنزيمات الكبد، كما ذكرنا، فدواء زولجنسما من الممكن أن يقوم بزيادة مستويات إنزيم الكبد ويسبب إصابة الكبد الحادة أو الفشل الكبدي الحاد، وهذا سبب تلقي الطفل المريض للكورتيكوستيرويد من طريق الفم قبل أخذ دواء زولجنسما وبعده، وبالتالي يجب عمل اختبارات دم منظمة للطفل ومراقبة وظائف الكبد.
- قد يتغير لون جلد المريض بالاضافة إلى لون بياض العين إلى اللون الأصفر، فيجب حينها الاتصال بطبيب الطفل المختص على الفور، أو إذا فاتته جرعة من دواء الكورتيكوستيرويد أو تقيأها، أو إذا كان المريض يعاني من انخفاض في اليقظة.
لماذا يُكلف دواء زولجنسما 2.1 مليون دولار للجرعة الواحدة؟ ولماذا قد تُكلف بعض الأدوية هذا الكمّ الهائل من الأموال؟
لكي نفهم لماذا جرعة واحدة من الدواء تُكلف 2.1 مليون دولار؟ علينا أولاً أن نبدأ بالنظر في كيفية تصنيع الدواء ولماذا صُنِّع في المقام الأول.
دواء زولجنسما يندرج تحت فئة الطب الدقيق أو ما يُسمى (precision medicine) لأنه دواء يستهدف مشاكل معينة تنتج من الشفرة الجينية الفريدة للشخص، ويعتبر الطب الدقيق نقلة نوعية في العلاج، فهو أكثر فاعلية في علاج الأمراض من الطرق التقليدية.
بشكل أكثر تحديداً، يعتبر دواء زولجنسما - كما ذكرنا - أحد أنواع العلاج الجيني، حيث صُمِّم لاستهداف السبب الجيني لضمور العضلات الشوكي، وهو جين SMN1 المفقود أو غير الفعال، ما يعني أنه يحل محل الجين المفقود أو غير العامل ويستبدله بنسخة جديدة للجين فعالة وصالحة للعمل. ومع ذلك، ليس من السهل تسليم نسخة فعالة عاملة من الجين الى الخلية، حيث يجب وضع الجين الجديد داخل ناقل عبارة عن فيروس يُسمى AAV9 كما ذكرنا في آلية عمل الدواء.
وعلى الرغم من أن العلاج الجيني يعد خياراً علاجياً ذا فعالية كبيرة، بالإضافة إلى أنه يعطي أملاً لعلاج العديد من الحالات الطبية، إلا أن عملية تصنيع تلك الأدوية صعبة وباهظة الثمن، كذلك فإن الشركات تتنافس على تطوير الأدوية الجديدة وتسويقها، لكنها لم تقضِ الوقت الكافي لتحسين عملية الإنتاج، ونتيجة ذلك تدخل الأدوية الى السوق بسرعة، لكن تصنيعها غالي الثمن، فتنتقل التكلفة المرتفعة إلى المرضى.
إذاً، هل نُلقي اللوم على شركات الأدوية على تلك التكلفة الجنونية لبعض الأدوية؟ بالتأكيد، شركات الأدوية شركات ربحية. وبالفعل، تربح الشركات مبالغ خيالية. وبعض تلك الشركات تربح بطرق غير أخلاقية، لكن يجب علينا معرفة أنه من دون تلك الشركات، ومن دون المبالغ التي تُصرَف على البحث العلمي والتجارب، لم يكن باستطاعتنا الحصول على الدواء، ولا معالجة المرض، وكان الطفل الذي يُشخَّص بالمرض مصيره الموت للأسف.
إذاً السبب في ارتفاع تكلفة دواء زولجنسما، أن هذا هو السعر الذي قررت شركة نوفارتس (Novartis)، وهي الشركة المنتجة للدواء، هو السعر الذي يستحقه الدواء لأنه يحول بشكل كبير حياة العائلات المتضررة من هذا المرض المدمر، بالإضافة إلى التكلفة الغالية لجلب أدوية جديدة إلى السوق، حيث صرح الرئيس التنفيذي لشركة نوفارتس، فاس ناراسيمهان، بأن العلاجات الجينية تمثل طفرة طبية في الطريقة التي توفر بها الأمل في علاج الأمراض الوراثية القاتلة بجرعة واحدة، وفي بعض الحالات يكون البديل عبارة عن علاج متعدد الجرعات مع تحسينات تدريجية.
وفقاً لدراسة أجريت عام 2016 نُشرَت في مجلة اقتصاديات الصحة، أنه لكي يُخترَع دواء جديد واحد، فإن الأمر يستغرق حوالى 2.6 مليار دولار، وأكثر من 10 سنوات. وأشارت دراسة أخرى أجراها معهد ماساتشوستس للتكنولوجيا (MIT) إلى أن 14% فقط من الأدوية في التجارب السريرية تحصل في النهاية على موافقة الاستثمار الأجنبي المباشر، نظراً لعدم نجاح قدر كبير من الأبحاث الدوائية.
لا توجد أيضاً قدرة تصنيعية كافية في العالم لخدمة أي شيء سوى الأمراض النادرة أو النادرة جداً في الوقت الحالي ببساطة بسبب عملية الإنتاج، ولا توجد قدرة على التوسع، لأنه يجب عليك أن تشتري مواد باهظة الثمن لصنع أدوية العلاج الجيني، وفقاً لكلام الرئيس التنفيذي لشركة بيركلي لايتس، وهي شركة متخصصة في مجال التكنولوجيا الحيوية.
في النهاية، كيف تُحسَب التكلفة الفعلية للدواء؟ تستخدم العديد من الشركات نموذج تسعير قائماً على القيمة، الذي يحسب التكلفة بناءً على عدد سنوات العمر المكتسبة، بالإضافة إلى مراعاة فعالية الدواء. لكن هذا يعني وضع السعر بناءً على قيمة حياة شخص، بالإضافة إلى ضمان أن تحقق الشركة هامشاً معقولاً لاستثماراتها، ومن هنا نتطرق في حديثنا عن العدالة الأخلاقية في الطب. فعلى الرغم من أن دولة إنكلترا وفّرت دواء زولجنسما للأطفال الذين شُخِّصَت حالتهم بضمور العضلات الشوكي، إلا أن الكثير من الدول لم توفّر إلى الآن الدواء، وقد يكون السبب كيفية دفع هذا المبلغ الضخم لمعالجة طفل واحد فقط، ومن الممكن معالجة عشرات الأطفال بذات المبلغ، وبالتالي يعتبر خياراً صعباً على الدولة وعلى الميزانية المخصصة للصحة.
لكن أحد الحلول لتوفير الدواء وتقليل ثمنه قد يكون مشاركة الدولة شركات الأدوية في تكاليف البحث العلمي والتجارب، حيث مُوِّل التطوير المبكر لدواء زولجنسما من قبل العديد من المؤسسات الخيرية الأميركية والمعاهد الوطنية للصحة، وكانت تستخدم العديد من هذه الجمعيات الخيرية تبرعات أسر المرضى وأصدقائهم لدعم الأبحاث والتجارب السريرية في الأدوية الجديدة لعلاج ضمور العضلات الشوكي.
هل هناك أدوية بديلة لدواء زولجنسما لعلاج ضمور العضلات الشوكي؟
- يوجد دواء نوسينرسين nusinersen تحت الاسم التجاري سبينرازا (Spinraza), أول دواء جرت الموافقة عليه للأطفال والبالغين المصابين بضمور العضلات الشوكي من قبل إدارة الغذاء والدواء الأميركية في ديسمبر 2016، وهو عبارة عن حقنة تُعطى في السائل المحيط بالحبل الشوكي. ويؤخذ دواء سبينرازا أربع مرات في السنة مدى الحياة، بتكلفة 750 ألف دولار للسنة الأولى، ثم 350 ألف دولار سنوياً بعد ذلك، أي حوالى 4 ملايين دولار لكل عقد.
- في أغسطس 2020، أعلنت إدارة الغذاء والدواء الأميركية إطلاق دواء ثالث يسمى دواء ريسديبلام risdiplam تحت الاسم التجاري (Evrysdi) لعلاج المرضى الذين لا تزيد أعمارهم على شهرين، وهذا الدواء هو الدواء الأول الذي يُتناوَل من طريق الفم لعلاج المرض.
المصادر
ZOLGENSMA targets the genetic root cause of SMA with a one-time dose